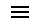胶囊的型号和大小(胶囊的型号和大小 图示)
胶囊的型号和大小怎么看
有8种,000号、00号、0号、1号、2号、3号、4号、5号、000号最大、5号最小、0号1号和2号比较常用。
胶囊的型号和大小 图示
来自:中国医*包装协会整理:了了
明胶空心胶囊
Vacantgelatincapsules
(征求意见稿)
目录
前言
范围
规范性引用文件
规格品种
要求试验方法
检验规则
判定规则
包装、标识、运输、贮存
附录A胶囊用明胶
前言
本标准编制所依据的起草规则为 GB/T1.1。
本标准代替 YBX-2000-2007《明胶空心胶囊》,与 YBX-2000-2007 相比,除编辑性修改外主要技术变化如下:
——对标准中检验项目顺序进行了调整;
——对引用标准的版本进行了更新(见 2 引用标准);——修改理化指标顺序,将崩解时限前置(见表 1 理化指标要求);——增加生产过程中若有灭菌操作或者抑菌剂添加需按照*典进行相关检测(见 4.1 理化指标)。——修改“松紧度”标准,调整至≤1(见表 1 理化指标要求);
——修改“亚硫酸盐(以 SO2 计)”标准,调整至≤100(见表 1 理化指标要求);——修改透明胶囊的“炽灼残渣”标准,调整至≤2.0(见表 1 理化指标要求);——删除“凝冻强度”(见表 1 理化指标要求);
——修改“重金属(以 Pb 计)”标准,调整至≤40(见表 1 理化指标要求);——修改“微生物限度”检验项目(见 4.2 微生物限度);——修改“鉴别”检验方法及判定标准(见 5.1 鉴别);——修改“崩解时限”检验方法及判定描述(见 5.2.2 测定步骤);——修改“松紧度、亚硫酸盐(以 SO2 计)、重金属(以 Pb 计)”相应判定标准和检测方法(见 5.3 松紧度、5.5 亚硫酸盐(以 SO2 计)、5.8 重金属(以 Pb 计)); ----修改了“铬”检测方法(见 5.9 铬); ----删除了规格尺寸及外观质量,该部分内容将单独形成协会标准发布; ----删除了粘度及粘度试验方法,改为控制原料黏度;——修改“包装”描述,明确了对包装材料的要求(见 8.1 包装)——修改“贮存”描述,删除了保质期(见 8.4 贮存)
——删除原附录 A 试验方法,纳入标准正文,增加新附录 A 胶囊用明胶;——删除了附录 B 铬的检测(分光光度法);
1 范围
明胶空心胶囊
本标准规定了明胶空心胶囊的规格品种、技术指标及要求、试验方法、检验规则、判定规则以及产品包装、标识、运输、贮存的要求。
本标准适用于胶囊用明胶加辅料制成的明胶空心硬胶囊,胶囊用明胶应符合附录 A 要求。
2 规范性引用文件
下列文件对于本标准的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本标准。
《中华人民共和国*典》2015 年版
GB/T2828.1-2012 计数抽样检验程序
GB6783-2013 食品安全国家标准食品添加剂明胶 T/CNPPA****―**** 空心胶囊规格尺寸及外观质量
3 规格品种
明胶空心胶囊(以下简称为“胶囊”)呈圆筒状,系由帽和体两节套合的质硬且具有弹性的空囊,具有不同的锁合结构。
3.1 规格
胶囊按其容量大小分为 00#、0#、1#、2#、3#、4#、5#及其他特殊规格型号,常规加长型胶囊以 el 表示,例:0#el。具体规格尺寸及外观要求参照中国医*包装协会标准《空心胶囊规格尺寸及外观质量》执行,特殊规格型号可由生产企业自行制定企业标准。
3.2 品种
胶囊分为透明(两节均不含遮光剂)、不透明(两节均含遮光剂)、半透明(仅一节含遮光剂)三种。
4 要求
4.1 理化指标
表 1 给出了胶囊理化指标要求。
表 1 理化指标要求
项目
单位
指标
鉴别
—
应符合规定
崩解时限≤
min
10
松紧度≤
粒
1
脆碎度≤
粒
2
亚硫酸盐(以 SO2 计)≤
mg/kg
100
干燥失重
%
13.0~17.0
炽灼残渣
透明≤
%
2.0
半透明≤
3.0
不透明≤
5.0
重金属(以 Pb 计)≤
mg/kg
40
铬≤
mg/kg
2
若生产过程使用环氧乙烷灭菌或添加对羟基苯甲酸酯类抑菌剂,应按照《中华人民共和国*典》规定增加相应项目的检测和控制。
4.2 微生物限度 微生物限度应符合表 2 规定。
表 2 微生物限度
项目
单位
指标
需氧菌总数≤
cfu/g
1000
霉菌和酵母菌总数≤
cfu/g
100
大肠埃希菌
/g
不得检出
沙门菌
/10g
不得检出
4.3 颜色 色泽均匀,有光泽,同一批产品无明显色差。
5 试验方法
51 鉴别
5.1.1 试剂
5.1.1.1 重铬酸钾试液。
5.1.1.2 稀盐酸。
5.1.1.3 鞣酸试液。
5.1.1.4 钠石灰。
5.1.1.5 石蕊试纸。
5.1.2 测定步骤
5.1.2.1 取本品 0.25g,加水 50ml,加热使溶化,放冷,摇匀,取溶液 5ml,加重铬酸钾试液-稀盐酸(4:1)数滴,即生成絮状沉淀。
5.1.2.2 取 5.1.2.1 项下的溶液 1ml,加水 50ml,摇匀,加鞣酸试液数滴,即发生浑浊。
5.1.2.3 取本品约 0.3g,置试管中,加钠石灰少许,加热,产生的气体能使湿润的红色石蕊
试纸变蓝色。
5.2 崩解时限
5.2.1 仪器及辅料
5.2.1.1 崩解时限测定仪:可控温度(37±1)°C。 5.2.1.2 滑石粉
5.2.2 测定步骤
取胶囊6粒,装满滑石粉(滑石粉装满程度以胶囊不漂浮于水面为准),锁合,分别置于吊篮的玻璃管中,加挡板,按照《中华人民共和国*典》崩解时限检查法(通则0921)胶囊项下的方法,各粒均应在10分钟内全部崩解或溶化,除破碎的胶囊壳外,应全部通过筛网。允许有胶囊碎片存在。如有少量不能通过筛网,但已软化或轻质上漂且无硬心者,可作符合规定论。如有1粒不能崩解,应另取6粒复试,均应符合规定。
5.3 松紧度 5.3.1 仪器
木板:厚度2cm。 5.3.2 测定步骤
取胶囊 10 粒,用拇指和食指轻捏胶囊两端,旋转拔开,不得有粘结、变形或破裂现象,然后装满滑石粉,将帽、体锁合,逐粒在 1m 的高度处直坠于厚度为 2cm 的木板上,应漏粉;如有少量漏粉,不得超过 1 粒,如超过,应另取 10 粒复试,均应符合规定。
5.4 脆碎度
5.4.1 试剂及仪器
5.4.1.1 饱和硝酸镁溶液。
5.4.1.2 干燥器。
5.4.1.3 玻璃管:内经 24mm、长 200mm。
5.4.1.4 聚四氟乙烯圆柱形砝码:直径为 22mm,重(20.0±0.1)g。
5.4.1.5 木板:厚度 2cm。
5.4.2 测定步骤
取胶囊 50 粒,置表面皿中,移入盛有硝酸镁饱和溶液的干燥器内,置 25°C±1°C恒温 24h ,取出,立即分别逐粒放入直立在木板上的玻璃管内,将圆柱形砝码从玻璃管口处自由落下,视胶囊是否破裂,如有破裂,不得超过 2 粒。
5.5 亚硫酸盐(以 SO2 计)
5.5.1 试剂及仪器
5.5.1.1 长颈圆底烧瓶:500ml。
5.5.1.2 磷酸:分析纯。
5.5.1.3 碳酸氢钠:分析纯。
5.5.1.4 碘溶液:0.05mol/L。
5.5.1.5 标准硫酸钾溶液(每 1ml 相当于 0.1mg 的 SO42-):称取硫酸钾 0.181g,置 1000ml
量瓶中,加水适量使溶解并稀释至刻度,摇匀。 5.5.2 测定步骤准确称取胶囊 5.0g,置长颈圆底烧瓶中;加热水 100ml 使溶化,加磷酸 2ml、碳酸氢钠 0.5g,即时连接冷凝管,加热蒸馏,以 0.05mol/L 碘溶液 15ml 为接收液,收集馏出液 50ml,用水稀释至 100ml,摇匀,量取 50ml,置水浴上蒸发,随时补充水适量,蒸至溶液几乎无色,用水稀释至 40ml,置 50ml 纳氏比色管中,加稀盐酸 2ml,摇匀,作为供试溶液。另取 3.75ml 标准硫酸钾溶液,置 50ml 纳氏比色管中,加水使成约 40ml,加盐酸 2ml,摇匀,作为对照溶液。在供试溶液与对照溶液中分别加入 25%氯化钡溶液 5ml,用水稀释至 50ml,充分摇匀,放置 10min,同置黑色背景上,从比色管上方向下观察、比较,供试溶液不得比对照溶液更浑浊。
5.6 干燥失重
5.6.1 仪器
5.6.1.1 分析天平:精度 0.1mg。
5.6.1.2 干燥器。
5.6.1.3 干燥箱:可控温度在(105±2)°C。
5.6.1.4 称量瓶。
5.6.2 测定步骤
称取胶囊约 1.0g,精确到 0.1mg,置已干燥恒重的称量瓶中,将帽、体分开,在 105°C干燥箱中干燥 6h,取出加盖,移至干燥器中,放冷至室温,精密称定。
5.6.3 结果计算:
y= m1-m2 ×100% m1-m0
式中:
y——干燥失重,%; m1——称量瓶和试样干燥前的总质量,单位为克(g);
m2——称量瓶和试样干燥后的总质量,单位为克(g); m0——称量瓶质量,单位为克(g)。计算结果表示到小数点后一位。
5.6.4 精密度在重复性条件下获得的两次独立测定结果的绝对差值应不大于 0.4%。
5.7 炽灼残渣 5.7.1 仪器
5.7.1.1 高温炉:可控温度在(500~600)°C。
5.7.1.2 分析天平:精度 0.1mg。
5.7.1.3 瓷坩埚:50ml。
5.7.1.4 干燥器。
5.7.2 测定步骤
称取胶囊约 1.0g,精确至 0.1mg,置已炽灼恒重的坩埚中,缓缓炽灼至完全炭化,放冷至室温,加硫酸 0.5ml~1ml 使湿润,低温加热至硫酸蒸气除尽后在 600°C炽灼使完全灰化恒重,移至干燥器内,放冷至室温,精密称定。
5.7.3 结果计算:
d= m2-m0 ×100% m1-m0
式中:
d——炽灼残渣,%; m2——坩埚和试样灼烧后的总质量,单位为克(g); m0——坩埚质量,单位为克(g); m1——坩埚和试样灼烧前的总质量,单位为克(g)。计算结果表示到小数点后一位。
5.7.4 精密度在重复性条件下获得的两次独立测定结果的绝对差值应不大于 0.2%。
5.8 重金属(以 Pb 计) 5.8.1 试剂及仪器
5.8.1.1 盐酸、硝酸:分析纯。
5.8.1.2 氨试液:取浓氨溶液 400ml 加水使成 1000ml。
5.8.1.3 醋酸盐缓冲液(pH3.5):取醋酸铵 25.0g 溶于 25ml 水中,加 7mol/L 盐酸 38ml,用 2mol/L 盐酸溶液或 5mol/L 氨溶液准确调节 pH 至 3.5(电位法指示),用水稀释至 100ml。
5.8.1.4 酚酞指示液:取酚酞 1g,加乙醇 100ml 使溶解。
5.8.1.5 铅标准溶液(每 1ml 相当于 0.01mg 的 Pb):称取硝酸铅 0.160g,置 1000ml 量瓶中,加硝酸5ml与水50ml溶解后,用水稀释至刻度,摇匀,作为贮备液。临用前精密量取贮备液 10ml,置 100ml 量瓶中,加水稀释至刻度,摇匀。
5.8.1.6 硫代乙酰胺试液:取 4g 硫代乙酰胺加水使溶解成 100ml 置冰箱中保存。临用前取混合液[由 1mol/L 氢氧化钠溶液 15ml、水 5.0ml 及丙三醇 20ml 组成]5ml,加上述硫代乙酰胺溶液 1.0ml 置水浴上加热 20 秒钟,冷却,立即使用。
5.8.1.7 纳氏比色管:25ml。 5.8.2 测定步骤取炽灼残渣项下遗留的残渣,加硝酸 0.5ml 蒸干,至氧化氮蒸汽除尽后,放冷,加盐酸 2ml,置水浴上蒸干后加水 5ml,微热溶解,滤过(透明胶囊不需滤过),滤渣用 15ml 水洗涤,合并滤液和洗液至乙管中,对照同样操作,依法检查(中国*典 2015 年版通则 0821第二法)。
5.9 铬
取本品 0.5g,置聚四氟乙烯消解罐内,加硝酸 5~10ml,混匀,浸泡过夜,盖上内盖,旋紧外套,置适宜的微波消解炉内,进行消解。消解完全后,取消解内罐置电热板上缓缓加热至红棕色蒸气挥尽并近干,用 2%硝酸转移至 50ml 量瓶中,并用 2%硝酸稀释至刻度,摇匀,作为供试品溶液。若本品中含有遮光剂,应采用在添加硝酸后再加 0.5ml 氢氟酸或者对供试品溶液进行离心处理后取上清液作为供试液,排除对检测的影响。同法制备试剂空白溶液;另取铬单元素标准溶液,用 2%硝酸稀释制成每 1ml 含铬1.0μg的铬标准贮备液,临用时,分别精密量取铬标准贮备液适量,用 2%硝酸溶液稀释制成每 1ml 含铬 0~80ng 的对照品溶液。取供试品溶液与对照品溶液,以石墨炉为原子化器,照原子吸收分光光度法(中国*典 2015 年版通则 0406 第一法),在 357.9nm 的波长处测定,计算,即得。
5.9 微生物
按《中华人民共和国*典》2015 年版通则 1105 与 1106 进行检查。
6 检验规则 6.1 抽样
在检验外包装之后,从同一批号产品中,按表 6 规定,随机抽出一定件数进行取样。 表6 抽样件数
从抽出的每一件包装内分别取出等量样品,混合后形成样本,总量不少于 90g。
7 判定规则
收货方在验收时,任何一项技术指标达不到规定,应与生产厂家对该不合格项目进行会同检验,以会同检验结果判定合格或不合格。
8 包装、标识、运输、贮存
8.1 包装 产品内包装应采用符合食品级或*品级包装要求的包装材料,外包装采用瓦楞纸箱或由供需双方协商确定。
8.2 标识 产品标识应符合国家有关法规的相关要求。标识内容至少包括:生产企业名称、产品名称、批号、生产日期、有效期、执行标准、包装数量、运输及贮存条件等。
8.3 运输 产品在运输过程中应防压、防晒、防潮、防热。不可与有毒物品或腐败变质物品混在一起装运。
8.4 贮存 本产品必须密闭,贮存在清洁、干燥、通风的仓库中,不得露天堆放,贮存条件为相对湿度 35%~65%,温度为 10°C~25°C。
每批产品的包装件数
应抽样件数
2~15 件
2
16~50 件
3
51~150 件
5
151~500 件
8
附录 A
胶囊用明胶
本品为动物的皮、骨、腱与韧带中胶原蛋白不完全酸水解、碱水解或酶降解后纯化得到的制品,或为上述三种不同明胶制品的混合物。
A.1 性状
本品为微黄色至黄色、透明或半透明微带光泽的薄片或粉粒;无臭、无味;浸在水中时会膨胀变软,能吸收其自身质量 5~10 倍的水。
本品在热水中易溶,在醋酸或甘油与水的热混合液中溶解,在乙醇中不溶。
A.2 鉴别
A.2.1 取本品 0.5g,加水 50ml,加热使溶解,取溶液 5ml,加重铬酸钾试液-稀盐酸(4: 1)的混合液数滴,即产生橘黄色絮状沉淀。
A.2.2 取鉴别A.2.1项下剩余的溶液1ml,加水100ml,摇匀后,加鞣酸试液数滴,即发生浑浊。
A.2.3 取本品约0.3g,置试管中,加钠石灰少许,加热,产生的气体能使湿润的红色石蕊试纸变蓝色。
A.3 检查
A.3.1 冻力强度
取本品两份各 7.50g,分别置冻力瓶内,加水制成 6.67%的胶液,加盖,放置 1~4 小时后,在65°C±2°C的水浴中搅拌加热 15 分钟使供试品溶散均匀,在室温下放置 15 分钟后,将冻力瓶水平放置在10°C±0.1°C的恒温水浴中,用橡胶塞密塞保温17小时±1小时后,迅速移出冻力瓶,擦干外壁,置冻力仪测试台上测试,计算两次结果的平均值,冻力强度应不低于 180Bloomg。
A.3.2 酸碱度
取本品 1.0g,加入热水 100ml,充分振摇使溶解,放冷至35°C,依法测定(中国*典 2015 年版通则 0631),pH 值应为 4.0~7.2。
A.3.3 透光率
取本品 2.0g,加 50~60°C水溶解并制成含 6.67%的溶液后,冷却至45°C,照紫外-可见分光光度法(中国*典 2015 年版通则 0401),分别在 450nm 和 620nm 的波长处测定透光率,分别不得低于 50%和 70%。
A.3.4 电导率
取本品 1.0g,加不超过60°C的水溶解并制成含 1.0%的溶液,作为供试品溶液,另取水 100ml 作为空白溶液,将供试品溶液与空白溶液置于30°C±1°C的水浴中保温 1 小时后,用电导率仪测定,以铂黑电极作为测定电极,先用空白溶液冲洗电极 3 次后,测定空白溶液的电导率,其电导率值应不得5.0μS/cm。取出电极,再用供试品溶液冲洗电极 3 次后,测定供试品溶液的电导率,应不得过 0.5mS/cm。
A.3.5 亚硫酸盐(以SO2计)
取本品 10.0g,置于长颈圆底烧瓶中,加水 150ml,放置 1 小时后,在60°C水浴加热使溶解,加磷酸 5ml 与碳酸氢钠 1g,即时连接冷凝管(产生过量的泡沫时,可加入适量的消泡剂,如硅油等),加热蒸馏,用 0.05mol/L 碘溶液 15ml 作为接收液,收集馏出液 50ml,用水稀释至 100ml,摇匀,量取 50ml,置水浴上蒸发,随时补充水适量,蒸至溶液几乎无色,用水稀释至 40ml,照硫酸盐检查法(中国*典 2015 年版通则 0802)检查,如显浑浊,与标准硫酸钾溶液 7.5ml 制成的对照液比较,不得更浓(0.01%)。
A.3.6 过氧化物
取本品 10g,置 250ml 具塞烧瓶中,加水 140ml,放置 2 小时,在50°C的水浴中加热使迅速溶解,立即冷却,加硫酸溶液(1→5)6ml,碘化钾 0.2g,1%淀粉溶液 2ml 与 0.5%钼酸铵溶液 1ml,密塞,摇匀,置暗处放置 10 分钟,溶液不得显蓝色。
A.3.7 干燥失重
取本品,在105°C干燥15小时,减失重量不得过15.0(% 中国*典2015年版通则0831)。
A.3.8 黏度
A.3.8.1 仪器和试剂
a) 平氏黏度计管:φ2.0mm;
b) 水浴:可调温度 60°C±1°C;
c) 恒温培养箱:可调温度 60°C±1°C;
d) 烧杯:150ml;
e) 三角烧瓶:150ml;
f)恒温水浴:可调温度 40.0°C±0.1°C;
g)秒表:分度 0.2 秒。
A.3.8.2 测定步骤
称取 15.0g 样品于已知重量的 150ml 灭菌烧杯中,加冷却的灭菌水约 70ml,在室温下膨胀 2~3h,在 60°C±1°C水浴中溶解,取出,配成 15%的胶液[(100-水份)×15.0/15]g,用灭菌的 80 目筛网过滤,将滤液滤入 150ml 灭菌的三角瓶中,用毛细管黏度计倒置吸取溶液到规定刻度,将黏度计迅速倒转,擦去粘附于管外的溶液,垂直固定于恒温水浴中,并使水浴的液面高于测定球的中部,放置 15 分钟,吸取溶液超过测定球刻度线,使溶液在管内自然下落,用秒表准确记录液面自测定线 1 下降至测定线 2 的流出时间。重复 3 次以上,每次测定值与平均值的差值不得超过平均值的±0.25%。记录运动黏度 A1,结果计算:
A1(mm2/s)=Kt
式中:K——平氏黏度计的系数,mm2/s2;
t——胶液流出时间,s;。
平行测定结果之差不大于 2mm2/s,取其算术平均值作为报告结果。黏度不小于 70mm2/s。
A.3.9 黏度下降
将 A.3.8.2 盛有剩余胶液的三角瓶称重,瓶口塞以无菌棉花,在 60°C±1°C恒温箱培养
17h±1h,取出称重,补足失去的水份,然后测定运动黏度
A2,黏度下降计算:
黏度下降(%)= A1-A2 ×100%A1
式中:A1——样品原黏度,mm2/s;
A2 ——恒温培养 17h 后的黏度,mm2/s。
平行测定结果相差不大于 3%,取其算术平均值作为报告结果。黏度下降不大于 24%。
A.3.10 炽灼残渣
取本品 1.0g,依法检查(中国*典 2015 年版通则 0841),遗留残渣不得过 2.0%。
A.3.11 铬
取本品 0.5g,置聚四氟乙烯消解罐内,加硝酸 5~10ml,混匀,100°C预消解 2 小时后,盖好内盖,旋紧外套,置适宜的微波消解炉内,进行消解。消解完全后,取消解内罐置电热板上缓缓加热至红棕色蒸气挥尽并近干,用 2%硝酸转入 50ml 聚四氟乙烯量瓶中,并稀释至刻度,摇匀,作为供试品溶液;同法制备空白溶液;另取铬单元素标准溶液,用 2%硝酸稀释制成每 1ml 中含铬1.0μg的铬标准贮备液,临用时,分别精密量取适量,用 2%硝酸溶液制成每 1ml 含铬 0~80ng 的对照品溶液。取供试品溶液与对照品溶液,以石墨炉为原子化器,照原子吸收分光光度法(中国*典 2015 年版通则 0406 第一法)或电感耦合等离子体质谱法(中国*典 2015 年版通则 0412 第一法)测定。含铬不得过百万分之二。
A.3.12 重金属
取炽灼残渣项下遗留的残渣,依法检查(中国*典 2015 年版通则 0821 第二法),含重金属不得过百万分之三十。
A.3.13 砷盐
取本品 2.0g,加淀粉 0.5g 与氢氧化钙 1.0g,加水少量,搅拌均匀,干燥后,先用小火炽灼使炭化,再在 500~600°C炽灼使灰化完全,放冷,加盐酸 8ml 与水 20ml 溶解后,依法检查(中国*典 2015 年版通则 0822 第一法),应符合规定(0.0001%)。
A.3.14 微生物限度
取本品,依法检查(中国*典 2015 年版通则 1105 与中国*典 2015 年版通则 1106),每 1g 供试品中需氧菌总数不得过 1000cfu,霉菌和酵母总菌数不得过 100cfu,不得检出大肠埃希菌;每 10g 供试品中不得检出沙门菌。
A.4 贮藏
避光,密闭保存。
胶囊 型号
00#、0#、1#、2#、3#、4#
胶囊的型号和大小有关系吗
NJP-3800
全自动胶囊充填机
胶囊是什么原料做的?
胶囊的原料是明胶、纤维素、多糖及其他辅料。胶囊在临床上是指用特殊材料,如明胶、纤维素、多糖等制成的囊状物,把味苦或刺激性大的*粉按剂量装入胶囊中,便于吞服。其中,胶囊可分为硬胶囊与软胶囊。
硬胶囊,又称空心胶囊,由明胶加辅料制成。呈圆筒状,是由帽和体两节套合的质硬且具有弹性的空囊。分为透明、半透明、不透明三种。另外,根据原材料进行分类,硬胶囊又可以分为明胶胶囊(由两节精密加工的胶囊壳组成)和植物胶囊(用植物纤维素或水溶性多糖为原料制成)。
软胶囊是以明胶、甘油、水作为成膜材料,将液体*物经处理密封于其中而制成的一种胶囊剂。胶囊制品需在医生指导下服用,切勿自行服*。
NJP-1200
全自动胶囊充填机
空胶囊的规格与选用具体是怎样的?
国内外生产的空胶囊的规格已经标准化,我国*用明胶硬胶囊标准共分8个型号,分别是000、00、0、1、2、3、4、5号,其号数愈大,容积愈小。常用规格是0、1、2、3号4种。胶囊填充*物多用容积来控制其剂量,而*物的密度、结晶、粒度不同,所占的体积不同,故应按*物剂量所占的容积来选用适宜大小的空硬胶囊。
NJP-400
全自动胶囊充填机
胶囊型号与装量
空心胶囊型号分为:胃溶-00#、0#、1#、2#、3#、4#;肠溶-0#、1#、2#。
空心胶囊颜色、样式:可根据客户提供的样品色定制生产,常用有白色、奶黄、红黄、绿白等色。空心胶囊印字印商标图案,可提供环向、轴向、定向、不定向。
产品包括:铝塑(铝/铝)泡罩包装机、灌装封尾机、胶囊充填机、装盒机、*品包装自动生产线等
免费获取包装方案
13967796270
胶囊的规格型号
胶囊的容积对不同比重的内容物所填充的重量以(mg)所示: 型号胶囊的容积0.5g/(ml) 0.7g/(ml)1.0g/(ml)1.2g/(ml) 00#0.79395553790948 0#0.67335469670804 1#0.50250350500600 2#0.37185259370444 3#0.30150210300360 4#0.21105147210252 填充的灌装机类型不同和内容物的性质不同,胶囊填充的重量波动性较大,上示数据仅供参考。 空心胶囊厚薄度 型号单壁厚薄(mm) 基本尺寸极限偏差 00#帽0.12±0.01 体0.12±0.01 0#帽0.11±0.01 体0.10±0.01 1#帽0.10±0.01 体0.10±0.01 2#帽0.10±0.01 体0.10±0.01 3#帽0.09±0.01 体0.09±0.01 4#帽0.085±0.01 体0.085±0.01 空心胶囊切口长度、口部外径、套合长度和平均重量 型号切口长度(mm) 口部外径(mm)套合长度(mm)平均重量(mg)重量差异 00#帽11.4-12.0 7.63-7.7722.2-23.2120±7±6% 体19.8-决病攻旧思城陆20.47.31-7.45 0#帽10.7-11.37.57-7.7120.7-21.797±6±6% 体18.2-18.87.26-7.40 1#帽9.00-10.16.83-6.9718.5-19.576±6 ±6% 体16.2-16.86.56-6.70 2#帽8.60-9.206.28-6.4217.0-17.862±5 ±6% 体15.1-15.76.00-6.14 3#帽7.80-8.405.76-5.9015.0-15.850±5±8% 体13.3-13.95.50-5.64 4#帽6.90-7.505.25-5.3913.4-14.339±5±8% 体11.9-12.54.98-5.12 空心胶囊理想化标准 项目质量标准 松紧度(粒)≤2 脆碎度(粒)≤15 崩解时限(分钟)≤10(允许破碎的胶囊壳存在) 亚硫酸盐(以SO2计%)<0.02 氯乙醇(PPm)<25 干燥失重(%)12.5-17.5 炽灼残渣(%) 全透明<2.0 半透明或一节透明、另一节不透明<3.0 一节半透明、另一节不透明<4.0 不透明<5.0 重金属(PPm)≤50 粘度(mm2/s)≥60 细菌总数(个/克)<1000 霉菌总数(个/克)<100 大肠杆菌不得检出 活螨不得检出 冻力(g)>180 空心胶囊外观质量标准 项目质量标准 颜色参照样品 目视缺陷A类AQL(%)2.5 目视缺陷B类AQL(%)4.0 目视缺陷C类AQL(%)6.5 印字缺陷A类AQL(%)2.5 印字缺陷B类AQL(%)4.0
胶囊的规格是什么意思
00#容量0.95ml0#容量0.75ml1#容量0.55ml2#容量0.40ml3#容量0.30ml4#容量0.25ml5#容量0.15ml
胶囊的型号和大小有区别吗
我国*用明胶硬胶囊标准规格共分8个型号,分别是000、00、0、1、2、3、4、5号。
其号数愈大,容积愈小。常用规格是0、1、2、3号4种。胶囊填充*物多用容积来控制其剂量,而*物的密度、结晶、粒度不同,所占的体积不同,故应按*物剂量所占的容积来选用适宜大小的空硬胶囊。
*物的重要性如下:
1、*物在人类生活中扮演着非常重要的角色。它们不仅可以治疗疾病,缓解疼痛,还可以预防疾病,提高人们的健康水平。*物对于疾病的诊断、治疗、预防以及疼痛缓解等方面都具有不可替代的作用。
2、首先,*物可以诊断疾病。许多疾病需要通过*物来进行诊断。例如,一些抗生素可以用来诊断肺炎等疾病。通过使用这些*物,医生可以观察患者的反应来确定他们是否患有这种疾病。此外,还有一些*物可以帮助医生更准确地诊断疾病,如某些抗癌*物和激素类*物。
3、其次,*物在治疗疾病方面具有重要作用。无论是细菌感染、病毒感染还是其他各种疾病,都可以通过使用适当的*物进行治疗。这些*物可以缓解症状,减轻疼痛,提高患者的生活质量。此外,*物还可以预防疾病。许多*物可以预防疾病的发生。
4、例如疫苗可以预防多种疾病。疫苗是一种经过处理过的病毒或细菌,它们可以刺激身体产生免疫力,从而预防疾病的发生。此外,还有一些*物可以预防心血管疾病、糖尿病等慢性疾病的发生。最后,*物还可以缓解疼痛。
5、疼痛是许多疾病的症状之一,而*物可以帮助缓解疼痛。例如,非处方*如阿司匹林和布洛芬等可以缓解轻度到中度的疼痛,而麻醉*可以缓解更严重的疼痛。
胶囊型号与大小
脑肽胶囊规格0.25g*12粒/板*2板/盒,我去店里看到的就是这种规格的呢!望可以帮到你呢
- 途观氙气灯泡型号(途观氙气灯泡型号规格)
- 产品型号4g(产品型号48v20ah怎么解释)
- 长城h5电瓶型号(长城h5电瓶型号及价格)
- 天逸功放哪种型号最好(天逸功放哪种型号最好用)
- 创酷火花塞型号(创酷火花塞型号怎么看)
- s6直屏型号(s6什么屏幕)
- 自吸磁力泵型号(自吸磁力泵型号大全)
- s6平面型号(s6 尺寸)
- 压路机有哪些型号(压路机有哪些型号规格)
- tcl电视什么型号的好(tcl电视什么型号的好用)
- 外径30内径15轴承型号(外径30内径15轴承型号厚9mm)
- 贝亲奶嘴最大什么型号(贝亲奶嘴的型号)
- ps4有几个型号(ps4几个型号的区别)
- 魅蓝a5型号(魅蓝 a5)
- s7港版型号(s7+ 港版)
- 护栏网规格型号(护栏网的用途)